Резюме
В обзоре приводится описание препаратов зверобоя и валерианы, результатов клинических исследований, посвященных изучению эффективности и безопасности применения данных препаратов при тревожно-депрессивных расстройствах.
Введение
В современном обществе люди сталкиваются лицом к лицу с множеством испытаний для психики: постоянные стрессы на работе и дома, спешка, ограниченное время для сна, эмоциональные переживания, всё это создает перманентную нагрузку на нервную систему. Благодаря активизации адаптивных механизмов в головном мозге какое-то время удается справляться со всеми этими нагрузками. Однако нередко эти механизмы истощаются или не включаются вообще, что может приводить к появлению тревоги, изменению общего эмоционального фона и настроения, которые могут стать началом тревожно-депрессивных расстройств. Стресс и, как следствие, депрессия являются в свою очередь немаловажным этиологическим фактором в снижении иммунитета и развитии многих соматических заболеваний - инсульта и инфаркта, язвенной болезни желудка и 12-типерстной кишки, артериальной гипертензии, гипотонии, стенокардии, бронхиальной астмы и многих других. Такие пациенты обращаются за консультацией к врачам различных специальностей, которые часто наблюдают недостаточную эффективность, казалось бы, правильно подобранного лечения. Причиной снижения эффективности лечения соматической патологии зачастую может быть нескорректированный психологический статус больного. Пациенты с легким депрессивным синдромом в подавляющем большинстве случаев выпадают из поля зрения врача и не получают необходимой терапии. Еще одной причиной в дополнение к сложностям диагностики является отрицательное отношение пациентов к антидепрессантам и психотропным препаратам, а также нежелание врачей назначать антидепрессанты из-за их побочных эффектов.
Европейское региональное бюро ВОЗ опубликовало в Health Evidence Network данные самого крупного систематического обзора материалов исследований, наблюдений и мета-анализов работ, в которых изучается влияние психосоциальных факторов на развитие не только сердечно-сосудистых, но и онкологичесских заболеваний. В частности данная работа содержит доказательства ассоциации ССЗ с депрессией (38). Данные других исследований говорят о наличии взаимосвязи между бронхиальной астмой и депрессивными расстройствами. Специалисты отмечают более высокую заболеваемость бронхиальной астмой среди больных с тревожным синдромом. Например, Koltek и соавт. обнаружили большую частоту астмы среди подростков с посттравматическим стрессовым расстройством (36). Ortega и соавт. в исследовании с участием 1285 молодых людей с бронхиальной астмой, также нашли более высокие показатели социально-психологических расстройств по сравнению с их сверстниками, не страдающими данной патологией (37).
С другой стороны, существует проблема соматизации тревожно-депрессивных расстройств, которая активно изучается во многих зарубежных исследованиях. Пациенты, имеющие такие расстройства субъективно оценивают общее ухудшение состояния своего здоровья и тяжесть соматического заболевания неадекватно высоко по отношению к данным объективных исследований. Они часто недовольны качеством медицинского обслуживания, обращаются к нескольким врачам по поводу одних и тех же жалоб. Получив подтверждение наличия у них соматического заболевания, такие пациенты отказываются признавать необходимость коррекции психологических расстройств, не соглашаются принимать синтетические антидепрессанты и часто остаются резистентны к терапии их соматической патологии. По данным Arthur J. Barsky и соавт. соматизированные больные в два раза чаще обращаются за медицинской помощью, и их лечение обходится в два раза дороже в сравнении с пациентами с аналогичными диагнозами без психологических проблем. Симптомы этих пациентов являются незначительными, однако они приводят к выраженной дисфункции, длительным периодам нетрудоспособности и даже инвалидности, что вносит еще и экономическую составляющую в данную проблему (35).
Таким образом, взаимосвязь тревожно-депрессивного синдрома с соматической патологией, утяжеление состояния больного при наличии такого сочетания диктует необходимость врачам различных профилей учитывать психическое здоровье пациентов при лечении их соматических заболеваний.
На сегодняшний день предпочитаемыми вариантами терапевтического воздействия при тревожных и депрессивных расстройствах являются когнитивно-поведенческая терапия и фармакологические агенты. Для лечения краткосрочных тревожных расстройств применяются бета-блокаторы и бензодиазепины, тогда как для терапии хронических состояний – селективные ингибиторы обратного захвата серотонина (СИОЗИС), селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) и ингибиторы моноаминооксидазы (МАО). Однако эти препараты часто имеют выраженные побочные эффекты в виде изменений когнитивной сферы (в случае применения бензодиазепинов [1]) или проблем с сердечно-сосудистой системой (в случае применения ингибиторов обратного захвата серотонина [2]). Кроме того нельзя не учитывать отношение пациентов к назначаемым препаратам, т.к. негативное отношение в сочетании с возможностью развития побочных эффектов становится препятствием в достижении желаемого результата.
Альтернативой этому могут являться препараты растительного происхождения, которые обладают сходными эффектами, но, при этом, практически лишены побочных явлений. Пациенты проявляют значительно более высокую готовность использовать растительные препараты, чем синтетические антидепрессанты. Так, по данным крупного популяционного исследования, проведенного в США, использование препаратов растительного происхождения выросло с 34% в 1990 году до 42% в 1997 году [3] и их применение продолжает расти. При этом их использование было почти вдвое больше у лиц с тревогой и депрессий, чем с какой-либо другой патологией. Врач, назначая такому больному средства растительного происхождения для коррекции психологического статуса, практически сводит к нулю возможное развитие побочных эффектов терапии при высокой их эффективности в борьбе с легкими тревожно-депрессивными расстройствами.
Особую важность использование растительных препаратов приобретает в лечении соматоформных расстройств. Проблема лечения пациентов с расстройствами этой группы чрезвычайно актуальна и является предметом изучения многих научных работ. Прежде всего, это связано с их высокой распространенностью: 12-месячная распространенность в европейской популяции составляет в среднем 6,3% с колебаниями в пределах 1,1–11% в зависимости от страны, в которой проводили исследование [39]. По данным обзора 26 крупных рандомизированных исследований с общим участием 2159 пациентов натуральные препараты в большей степени, чем плацебо, снижали соматические симптомы и тревогу у больных с соматоформными расстройствами. Тогда как курс лечения трициклическими антидепрессантами длительностью 6–12 недель уменьшал выраженность соматических симптомов не в большей степени, чем плацебо.
В последние годы появилось огромное количество исследований на тему применения препаратов растительного происхождения для лечения легкой и умеренной тревожности, тревожно-депрессивных расстройств, нарушений сна. В данном обзоре освещены некоторые существующие данные о препаратах зверобоя и валерианы и результаты их применения в лечении тревожно-депрессивных расстройств.
Зверобой (Hypericum perforatum)
Экстракты зверобоя применяются в медицине многие века и уже давно доказали свою эффективность в многочисленных современных исследованиях. Экстракт зверобоя содержит минимум 10 биологически активных веществ. К ним относятся феноловые кислоты (хлорогеновая кислота), флаваноиды (кверцетин, кверцитрин, изокверцитрин, рутин, гиперозид, эпигенанин), производные флороглюцинола (гиперфорин, адгиперфорин) и нафтодиантроны (гиперицин, псевдогиперицин) (рис. 1).
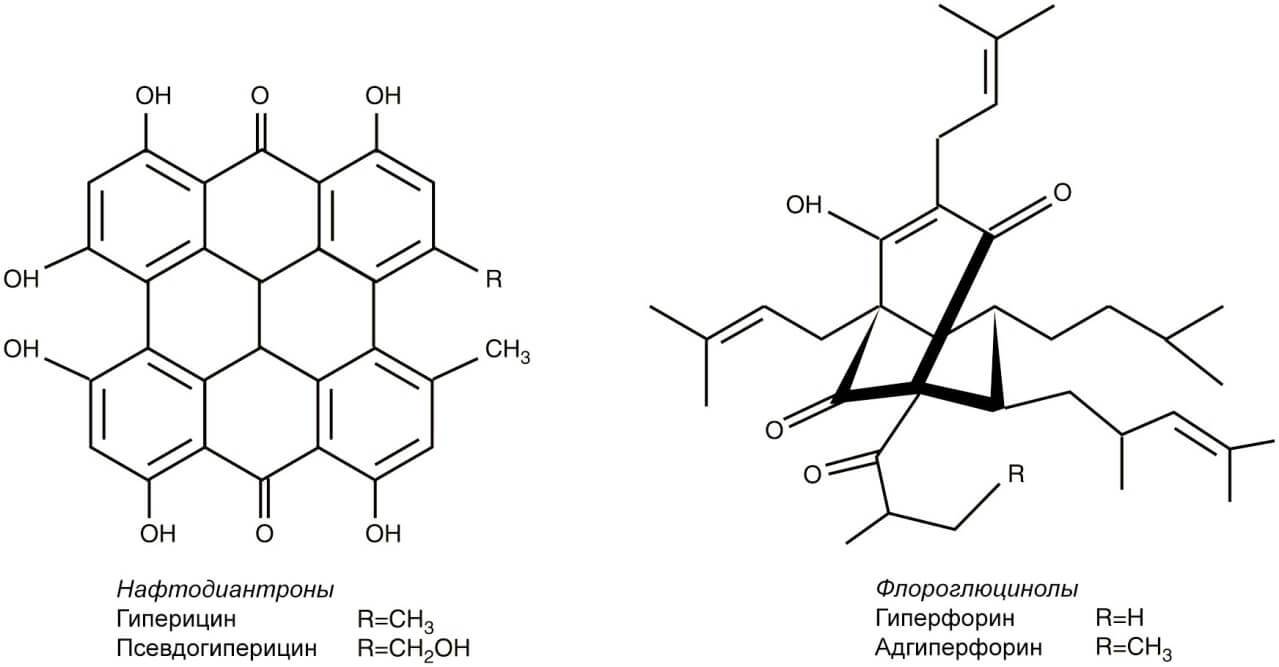
Рисунок 1. Некоторые биологически активные вещества, содержащиеся в экстракте зверобоя.
До недавнего времени считалось, что антидепрессивные и противовоспалительные свойства зверобоя связаны с нафтодиантронами [5], однако данные новых исследований показали, что в реализации этого механизма также играют значительную роль гиперфорин [6,7] и производные флаваноидов [8]. Сейчас принято считать, что различные эффекты зверобоя реализуются через суммацию и синергетическое действие всех его компонентов [9,10]. В исследовании антидепрессивных свойств экстракта зверобоя на молекулярном уровне было показано, что данная функция реализуется в ЦНС через ингибирование обратного захвата серотонина (эффект подобный антидепрессантам из группы СИОЗС), дофамина, норадреналина, ГАМК и L-глютамата [11]. В экспериментальном исследовании был показан нейропротективный эффект экстракта зверобоя и его способность улучшать когнитивную функцию [12]. В другом лабораторном исследовании, проведенном Tian с коллегами и опубликованном в 2014 году [13], была установлена роль адгиперфорина – недавно обнаруженного нового активного компонента экстракта зверобоя, в реализации мощной антидепрессантоподобной активности. По данным авторов, данный механизм реализовывается через ингибирование обратного захвата серотонина, дофамина и норадреналина, а также высокую аффинность связи с переносчиками серотонина и норадреналина. (рис.2)
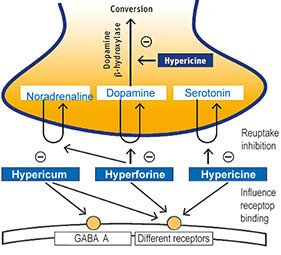
Рисунок 2. Механизм антидепрессивного действия зверобоя.
Большинство клинических исследований у людей на сегодняшний день сфокусировано на антидепрессивных свойствах экстракта зверобоя. Так в ряде систематических обзоров литературы и мета-анализов была подтверждена эффективность экстракта зверобоя в лечении легкой и умеренной депрессии [14]. В рандомизированном клиническом исследовании (РКИ) экстракта зверобоя при соматоформных расстройствах, сопровождающихся высокими уровнями тревоги [15], был показан значительный положительный эффект экстракта зверобоя по сравнению с плацебо в уменьшении соматической и психической тревоги, общего балла тревожности и выраженности симптомов соматоформного расстройства. В последнем Кокрановском обзоре, проведенном Linde с соавторами в 2008 году, анализировались данные 29 методологически идентичных контролируемых клинических исследований [16], в 18 из которых эффективность и безопасность экстракта зверобоя сравнивалась с плацебо, в 17 – со стандартной терапией синтетическими антидепрессантами. Общее число пациентов, участвующих в исследованиях составило 5489. Основным показателем оценки эффективности принимался относительный коэффициент положительного эффекта от лечения, показывающий, во сколько раз чаще эффект от лечения был достигнут при использовании экстракта зверобоя по сравнению с использованием средств сравнения. Эффективной терапия считалась при достижении ремиссии. По данным 8 крупных исследований этот коэффициент для экстракта зверобоя по сравнению с плацебо составил в среднем 1,28 (от 1.1 до 1, 47, доверительный интервал 95%), т.е в среднем ремиссия была достигнута в 1,28 раз (на 28%) чаще при лечении экстрактом зверобоя, чем при применении плацебо. В 9 более мелких исследованиях коэффициент был 1,87 (от 1,22 до 2,87, ДИ 95%), т.е эффективность зверобоя в этих исследованиях превышала эффективность плацебо практически в 2 раза.
При оценке эффективности зверобоя в сравнении с антидепрессантами результаты всех исследований были однородны. По сравнению с три - или тетрациклическими антидепрессантами и селективными ингибиторами обратного захвата серотонина (СИОЗС) соответственно, коэффициент эффективности был 1.02 (95% ДИ, от 0.90 до 1.15 по данным 5 исследований) и 1,00 (95% ДИ, от 0.90 до 1.11 по данным 12 исследований), т.е. количество пациентов, достигших ремиссии было одинаковым в обеих группах.
Безопасность препарата оценивалась путем сравнения числа пациентов, прекративших лечение из-за развития нежелательных эффектов. В группе больных, принимавших зверобой, прекратили лечение достоверно меньше пациентов, чем в группе принимавших антидепрессанты. Коэффициент сравнении для трициклических антидепрессантов составил 0,24 (ДИ 95%, от 0,13 до 0,46) и для СИОЗС - 0,53 (ДИ 95%, от 0,34 дл 0,83), т.е. пациенты, принимавшие экстракт зверобоя, прекращали лечение в связи с развитием нежелательных эффектов в 4 раза реже по сравнению с пациентами в группе трициклических антидепрессантов и в 2 раза реже по сравнению с СИОЗС.
Таким образом, данные клинических исследований говорят о том, что экстракт зверобоя более эффективен, чем плацебо и также эффективен, как синтетические антидепрессанты, в лечении депрессивных расстройств при достоверно меньшем количестве побочных эффектов, чем у последних.
Валериана (Valeriana officinalis)
Первые упоминания о валериане уходят своими корнями далеко в историю. Известно, что еще во II веке нашей эры Клавдий Гален применял валериану для лечения бессонницы. Однако применение препаратов валерианы сегодня основывается на данных современных исследований.
В состав валерианы входит более 150 биологически активных веществ [17,18,19], которые можно разделить на несколько групп: бициклические монотерпены (валепотриаты – вальтарат и дигидровальтрат), летучие масла (валеранон, валеренал, валереновая кислота), сесквитерпены, лигнаны, алкалоиды, аминокислоты (ГАМК, тирозин, аргинин, глютамин) (рис. 2). Ранее считалось, что валепотриаты, открытые еще в 1966 годы, являются единственным биологически активным компонентом, оказывающим терапевтическое действие, однако позже, с выявлением новых молекул, данная точка зрения изменилась [20]. Компоненты, входящие в состав валерианы, действуют синергично и дополняют друг друга [21,22].
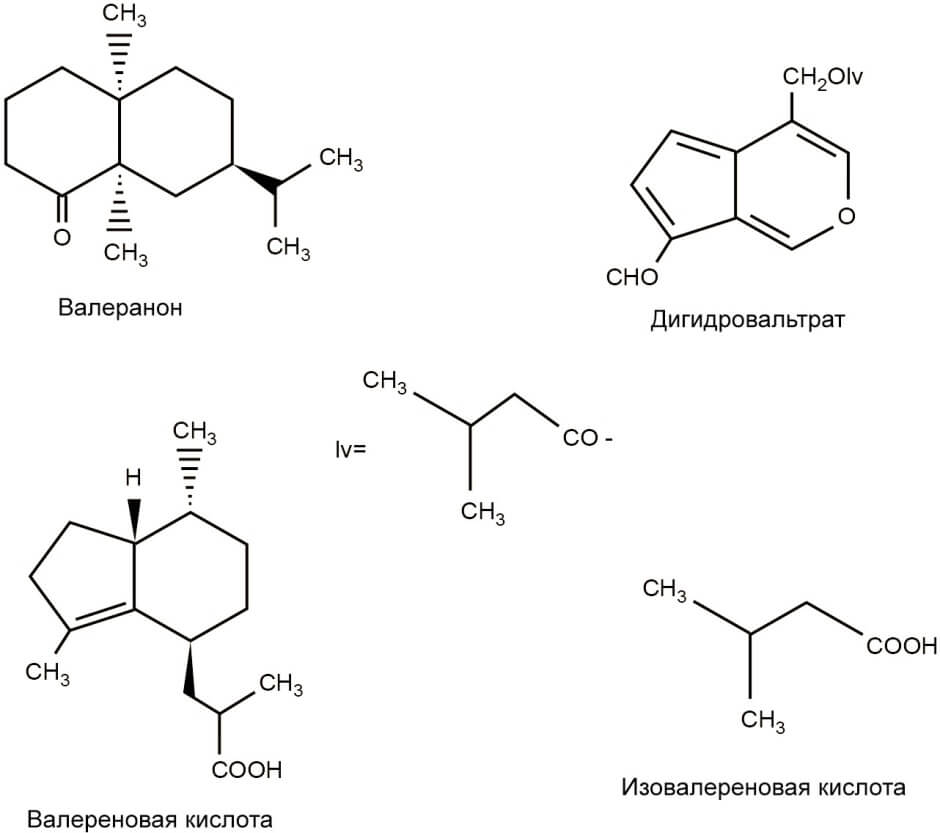
Рисунок 3. Некоторые биологически активные вещества, содержащиеся в экстракте валерианы.
Известно, что компоненты валерианы связываются с множеством нейротрансмиттерных рецепторов [23], включая серотониновые 5-HT5A рецепторы [24], что имеет эффект на циркадные ритмы и уровень тревоги. Компоненты валерианы также являются аллостерическими модуляторами субъединице-специфических ГАМКА каналов [25] и аденозиновых А1 рецепторов [26]. В экспериментальных исследованиях был установлен выраженный анксиолитический эффект [27], обусловленный связыванием валереновой кислоты и ее производных со специфической бета-3 субъединицей ГАМКА рецептора [28]. Компоненты валерианы также подавляют фермент-индуцированный распад ГАМК, оказывая, таким образом, седативный эффект [29]. В исследовании Bodesheim с коллегами было показано, что компонент валерианы гидроксипинорезинол имеет свойство связываться с бензодиазепиновыми рецепторами [30].
В двойном слепом исследовании 48-ми взрослых испытуемых, помещенных в условия экспериментального социального стресса, применение экстракта валерианы уменьшало субъективное ощущение тревоги [31]. В другом рандомизированном плацебо-контролируемом исследовании было показано значительное снижение тревожности по Шкале тревоги Гамильтона через 4 недели при применении препаратов валерианы (80 мг/сут), сопоставимое с применением диазепама (6,5 мг/сут) [32].
От монотерапии к эффективной комбинации
На сегодняшний день в общетерапевтической практике большинство пациентов с соматической патологией имеют ту или иную степень выраженности тревоги и депрессии, нарушений сна, сниженный фон настроения. Разнообразие психовегетативных нарушений обуславливает необходимость воздействия не на какое-то одно клиническое проявление, а на весь симптомокоплекс, имеющийся у пациента. Именно данный факт привел к тому, что в Германии, где культура использования растительных препаратов особенно высока, стали применять комбинацию экстракта зверобоя и экстракта валерианы. Процесс изготовления фитопрепаратов происходит в соответствие со строгими принципами стандартизации и с использованием методов, указанных в национальной фармакопее. Это означает, что препараты растительного происхождения соответствуют таким же строгим критериям качества, эффективности и безопасности, как и синтетические лекарственные средства.
В Германии с 1980 года было проведено более 350 клинических исследований с применением стандартизированных фитопрепаратов. В этих исследованиях изучалась эффективность препаратов растительного происхождения при лечении различных заболеваний легкой или средней степени тяжести или профилактики последних. Некоторые сравнительные исследования показали, что препараты растительного происхождения имеют полную терапевтическую эквивалентность с химически синтезированными препаратами, не имея при этом побочных эффектов. Механизм действия таких фитопрепаратов, содержащих, в отличие от синтетических агентов, несколько активных компонентов, характеризуется как поливалентный, а в некоторых случаях, как потенцирующий.
Примером удачной комбинации экстрактов зверобоя и валерианы является препарат СЕДАРИСТОН, производимый в Германии. Он содержит 100 мг сухого экстракта травы зверобоя 90% и 50 мг сухого экстракта корневищ с корнями валерианы. В различных исследованиях было показано, что такая комбинация превосходит по эффективности мототерапию этими препаратами, за счет комплексного и взаимопотенцирующего эффекта. Так, в открытом исследовании экстракта зверобоя в комбинации с экстрактом валерианы в лечении тревожно-депрессивных расстройств [33] было показано, что такая комбинации более эффективна, чем монотерапия экстрактом зверобоя; отмечалось значительное уменьшение тревожности при практически отсутствующих побочных эффектах.
В другом двойном слепом рандомизированном исследовании была показана более высокая эффективность стандартизированного экстракта зверобоя и валерианы в составе препарата СЕДАРИСТОН в лечении пациентов с тревожными состояниями средней степени тяжести по сравнению с диазепамом в низкой дозе 4-6 мг в сутки [34].
Немецкие ученые Hiller K., Rahlfs V. в двойном слепом рандомизированном контролируемом исследовании также оценили эффективность СЕДАРИСТОНа в сравнении с амитриптилином при лечении больных с диагнозом дистимия, короткие или более длительные депрессивные реакции, неврастения или невротическая депрессия (n=153). Пациенты группы СЕДАРИСТОНа получали по 1 или 2 капсулы 3 раза в сутки. Амитриптилин назначался в дозировке 25 или 50 мг 3 раза в сутки. Продолжительность лечения в обеих группах составила 6 недель. Оценка уровня депрессии производилась по шкале Гамильтона. Положительный эффект был достигнут у 82% в группе СЕДАРИСТОНа и у 77% - в группе амитриптилина. Суммарная оценка по шкале Гамильтона сократилась с 24,2 до 8,4 баллов после лечения СЕДАРИСТОНом и с 24,3 до 8,9 баллов после лечения амитриптилином. Результаты этого исследования доказывают, что эффективность СЕДАРИСТОНа при лечении тревожно-депрессивных расстройств не уступает эффективности амитриптилина. При этом СЕДАРИСТОН показал гораздо более высокий профиль безопасности. Его применение не сопровождалось развитием таких побочных явлений, как сонливость, перепады настроения и т.д.
Превосходящая эффективность указанной фитокомбинации объясняется не только анксиолитической составляющей действия ее растительных компонентов, но также повышающим настроение эффектом зверобоя. На сегодняшний день СЕДАРИСТОН является единственным в Украине зарегистрированным препаратом, содержащим как экстракт зверобоя, так и валерианы, что позволяет оказывать действие не только на тревожный компонент, но и на настроение.
Заключение
Препараты зверобоя и валерианы имеют большой потенциал для практического применения. По данным разных клинических исследований они обладают высокой эффективностью в лечении тревожно-депрессивных расстройств, сопоставимой с таковой у синтетических лекарственных препаратов, и хорошим профилем переносимости. Крайне низкая вероятность развития побочных эффектов позволяет врачам общего профиля без опасений назначать эти препараты при лечении больных с сопутствующими тревожно-депрессивными расстройствами. Отсутствие седативного эффекта при приеме СЕДАРИСТОНа позволяет использовать его у самого широкого круга пациентов, в том числе у водителей, работников различных машин и механизмов. Кроме того, полученные обнадеживающие результаты применения экстрактов зверобоя и валерианы в коррекции психологического статуса пациентов, позволяют врачам различных специальностей решить сразу две задачи: улучшить как психологическое, так и соматическое состояние пациентов.
Подготовили Романенко В.И., Романенко Ю.И., Романенко И.В.
Опубликовано в журнале «Международный эндокринологический журнал» №1(79)'2016


