Вступ
Синдром діабетичної стопи - одне з найрозповсюдженіших ускладнень цукрового діабету (ЦД). Це ускладнення є симптомокомплексом анатомо-функціональних ушкоджень, пов'язаних із дiабетичною мікроангіопатією, нейропатією, макроангіопатією судин нижніх кінцівок та остеоартропатією, що призводить до підвищеного травмування та інфікування м'яких тканин стопи, розвитку тяжких гнійно-некротичних-процесів i, внаслідок цього, до ампутації нижніх кінцівок [1]. Вперше діабетична стопа як самостійне ускладнення цукрового діабету була виділена у доповіді експертів ВООЗ з цукрового діабету відносно недавно - у 1987 році. У зв'язку з цим протягом останніх років в багатьох країнах світу йде напружена наукова та клінічна робота з вивчення цього ускладнення.
З'ясовано, що етіологія синдрому діабетичної стопи є багаточинниковою. Залежно від виду патологічного процесу вирізняють основні клінічні форми діабетичної стопи: нейропатичну, ішемічну та нейроішемічну. Залежно від стадій процесу виділяють субклінічну, клінічну, а також стадію пізніх ускладнень з наявністю неінфікованих та інфікованих поверхневих і глибоких виразок, стопи Шарко та нетравматичних спонтанних ампутацій. Най загрозливішим ускладненням діабетичної стопи є виразково-некротичні ураження, які стають без посередньою причиною ампутацій кінцівки. Згідно з проведеними епідеміологічними дослідженням частота трофічних уражень нижніх кінцівок складає близько 20%. З них приблизно 45% - нейропатичні виразки нижніх кінцівок, 52% - нейроішемічні та З% - ішемічні [3]. Слід зауважити, що тривалий час перед виникненням трофічного ураження, спричиненого здебільшого травмуванням стопи, синдром діабетичної стопи перебігає клінічно без симптомно, тому потребує активного виявлення лікарями та визначення факторів ризику Його розвитку, категорій пацієнтів, які потребують періодичного обстеження та лікування.
Згідно з сучасними уявленнями провідною причиною розвитку синдрому діабетичної стопи та наступної ампутації є діабетична полінейропатiя нижніх кінцівок. Остання та пов'язані з нею деформації стопи, а також втрата захисної больової чутливості призводять до виникнення спонтанних і травматичних виразкових дефектів м'яких тканин стопи з подальшим їх інфікуванням і розвитком гнійно-некротичного процесу. Діабетична полінейропатія нижніх кінцівок зі зниженою чутливістю підвищує ризик ампутації нижньої кінцівки в 1,7 рази, за умов наявності деформації стоп ризик ампутації збільшується в 12 разів, а за умов наявності виразки - в 36 разів [2]. У цілому ж діабетична полінейропатія нижніх кінцівок є основним чинником розвитку гангрени та ампутації нижньої кінцівки в 87% випадків [4].
Матеріали і методи
На базі відділу клінічної ендокринології Українського науково-практичного центру ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України було досліджено хворих на цукровий діабет 1 і 2 типів, у яких мала місце нейропатична форма синдрому діабетичної стопи. При цьому вивчалися демографічні дані (стать, вік, тривалість основного захворювання), анамнез, клінічні прояви та перебіг захворювання, стан компенсації вуглеводного та ліпідного обміну, визначався ступінь тяжкості нейропатії, і клінічні прояви, наявність виразково-некротичних уражень, їх походження (спонтанне або травматичне), на- явність супутньої макроангіопатії нижніх кінцівок, стан кісток стопи, наявність проявів мік- роангіопатії (зокрема, діабетичної ретиноатії), визначалися рівні С-пептиду та ендогенного інсуліну. Було також проведено дослідження ефективності та переносимості хворими різних доз альфа-ліпоєвої кислоти (600, 900 та 1200 мг на добу), яку використовували для етіотропного лікування нейропатії.
Всього були обстежені 73 хворих. На цукро- вий діабет I типу хворіли 22 пацієнти: 9 чоловіків та 13 жінок зі стажем діабету понад 10 років, середній вік захворювання складав 16+4,3 роки, середній вік хворих - 44,5+3,2 роки. На час обстеження всі хворі перебували у некомпенсованому стані, рівень глікованого гемоглобіну складав 9,3+0,8%, рівень глюкози натще - 10,2+1,9 ммоль/л, постпрандіальної 14,5+2,1 ммоль/л. Всі хворі мали виражені клінічні прояви нейропатії: нічні болі, судоми та слабкість у ногах - 17 пацієнтів (72,3%), зменшення вібраційної чутливості - 22 (100%), тактильної чутливості – 9 (40,9%), порушення больової чутливості – 7 (31,8%), зниження температурної чутливості – 12 (54,5%), порушення дискримінаційної чутливості - 14 (59,1%). Сухожильні рефлекси були знижені у 8 (36,4%) осіб, відсутні у 4 (18,1%) хворих. Скарг на болі в ногах при ходінні (переміжну кульгавість) не було в жодного хворого на ЦД I типу. Наявність трофічних уражень в анамнезі відзначали три (13,6%) пацієнти. Таким чином, типові скарги та об'єктивне обстеження виявили наявність клінічно значущої нейропатії в усіх хворих.
У 10 (45,4%) хворих цієї групи на момент обстеження мали місце виразково-некротичні дефекти, ступінь яких за Вагнером було розцінено як II-IV. У 2 хворих нейропатичну форму синдрому діабетичної стопи було ускладнено суглобом Шарко.
Аналіз кровообігу за допомогою допплерографії виявив, що у 4 (18,8%) пацієнтів мало місце порушення магістрального кровообігу на нижніх кінцівках з оклюзією та стенозом різних сегментів судин і зниженням кровопостачання на 50% і більше. Тобто нейропатична форма синдрому дiабетичної стопи мала місце у 72,2% хворих на ЦД I типу, а у 18,8% була змішана, нейроішемічна форма синдрому діабетичної стопи.
Група хворих із 2 типом ЦД включала 51 пацієнта (24 чоловіки та 27 жінок) віком від 48 до 81 року (середній вік - 64,3+4,5 роки). Тривалість захворювання була від 6 мiсяців до 33 років, в середньому 15,1+4,5 роки. Діабет у всіх хворих на час обстеження був у стані декомпенсації. Показники вмісту глікованого гемоглобіну, глюкози в крові натще та постпрандіальної наведені у таблиці 1.
Таблиця 1. Порівняльна характеристика хворих на цукровий діабет з нейропатичною формою синдрому діабетичної стопи
|
Показники |
ЦД 1 типу |
ЦД 2 типу |
|
Середній вік (роки) |
44,5 ± 3,2 |
64,3 ± 4,5 |
|
Середня тривалість ЦД (роки) |
16,8 ± 4,3 |
15,1 ± 4,5 |
|
HbAlc (%) |
9,3 ± 0,8 |
9,8 ± 0,6 |
|
Глюкоза натще (ммоль/л) |
10,2 ± 1,9 |
11,7 ± 0,5 |
|
Глюкоза постпрандіальна (ммоль/л) |
14,5 ± 2,1 |
12,9 ± 1,2 |
|
Наявність трофічних уражень кінцівки в анамнезі (%) |
13,65 ± |
21,5 |
|
Наявність болів у ногах при ходінні (%) |
- |
31,4 |
|
Наявність некротичної виразки (%) |
45,4 |
43,1 |
|
Віброметрія (ум.од.) |
2,1 ± 0,8 |
1,2 ± 0,4 |
|
Порушення тактильної чутливості (%) |
40,9 |
74,5 |
|
Порушення дискримінаційної чутливості (%) |
59,1 |
82,0 |
|
Порушення больової чутливості (%) |
31,8 |
39,2 |
|
Порушення температурної чутливості (%) |
54,5 |
72,5 |
|
Порушення сухожильних рефлексів (%) |
54,5 |
72,5 |
|
Наявність суглоба Шарко (%) |
9,1 |
9,8 |
|
Наявність остеопорозу в кістках стопи (%) |
- |
7,8 |
|
Наявність супутньої мікроангіопатії за результатами допплерографії (стеноз або оклюзія судин із зниженням кровообігу > 50%) (%) |
18,8 |
37,2 |
|
Наявність діабетичної ретинопатії |
72,3 |
58,8 |
На момент обстеження у всіх хворих виявлено клінічні ознаки нейропатії, які проявлялися скаргами на нічні болі, судоми та слабкість у ногах у 45 хворих (88,2%), зменшенням вібраційної чутливості у 51 (100%), тактильної чутливості у 38 (74,5%), порушенням больової чутливості у 24 (47%), зниженням температурної чутливості у 24 (47%), порушенням дискримiнаційної чутливості у 42 (82%) пацієнтів. Сухожильні рефлекси були знижені у 30 (58,8%) осіб, відсутні у 7 (13,7%) хворих. На болі при ходінні скаржилися 16 (31,4%) хворих на ЦД 2 типу. Наявність трофічних уражень в анамнезі відзначали 11 (21,5%) пацієнтів. Аналіз скарг та результатів об'єктивного обстеження засвідчив клінічно значущу нейропатію у всіх хворих та можливість наявності макроангіопатії нижніх кінцівок у 31,4% пацієнтів.
У 22 (43,1%) хворих з 2 типом ЦД і нейропатичною формою синдрому діабетичної стопи мали місце виразкові дефекти I-IV ступеня за Вагнером. Аналіз стану кровообігу за результатами допплерографії дозволив виявити наявність стенозу, оклюзії та порушення кровообігу і кровопостачання більше ніж на 50% у 19 (37,2%) хворих, на підставі чого в них діагностовано нейроішемічну форму синдрому діабетичної стопи. При цьому у 4 пацієнтів із стенозом, більшим за 75%, виявлено рентгенологічні ознаки остеомієлiту. Ці хворі в подальшому були переведені в хірургічний відділ для оперативного лікування. Суглоб Шарко мав місце у 5 (9,8%) осіб, у 4 (7,8%) за результатами рентгенологічного обстеження кісток стопи виявлено виражений остеопороз.
Порівняльний аналіз показників у хворих на ЦД 1 і 2 типів наведено у таблиці 1.
Для з'ясування факторів ризику та інших ознак, притаманних ускладненій виразкою формі діабетичної стопи у хворих з нейропатією, нами проведено аналіз стану хворих на діабет 1 і 2 типів з синдромом діабетичної стопи в залежності від наявності або відсутності виразково-некротичного процесу. Результати аналізу наведені в таблиці 2.
Таблиця 2. Аналіз стану хворих на ЦД 1 і 2 типів з синдромом діабетичної стопи, ускладненим та неускладненим виразково-некротичним процесом
|
Показники |
ЦД 1 типу, n=22 |
ЦД 2 типу, n =51 |
||
|
без виразки. n = 12 |
з виразкою. n = 10 |
без виразки. n =29 |
з виразкою. n =22 |
|
|
Співвідношення жін./чол. |
1:1 |
3:7 |
2:3 |
4:7 |
|
Вік (роки) |
36,7 ± 1,5 |
52,4 ± З,6* |
63,2 ±2,7 |
66,5 ±3,1 |
|
Тривалість ЦД (роки) |
13,6 ± 1,7 |
19,2 ±3,1* |
10,5 ±3,5 |
12,7 ±4,6 |
|
Віброметрія (ум.од.) |
3,6 ± 0,1 |
0,9 ± 0,03* |
2,1 ±0,4 |
0,19 ±0,08* |
|
Наявність макроангіопатії н.кінцівок (%) |
- |
40 |
37,9 |
86,4 |
|
Наявність діабетичної ретинопатії (%) |
41,6 |
100 |
24,1 |
50 |
|
Бета-ліпопротеїди (ммоль/л) |
1,31 ±0,2 |
3,5 ± 0,09* |
1,4 ±0,3 |
1,37 ± 0,4 |
|
Тригліцериди (ммоль/л) |
1,1 ±0,07 |
3,2 ± 0,3* |
3,5 ± 0,2 |
3,1 ± 0,3 |
|
Холестерин (ммоль/л) |
4,4 ± 0,2 |
7,6 ± 0,4* |
7,2 ± 0,3 |
7,1 ± 0,4 |
|
С-пептид (нг/мл) |
- |
- |
1,42 ±0,04 |
0,81 ±0,02* |
|
Ендогенний інсулін (нг/мл) |
- |
- |
0,42 ± 0,02 |
0,53 ± 0,02 |
Проведений аналіз продемонстрував, що група хворих на ЦД 1 типу з ускладненою формою синдрому дiабетичної стопи на 70% складається з чоловіків. Вік пацієнтів був від 40 до 67 років, тривалість захворювання - від 10 до 28 років. Обидва ці показники достовірно виші (р<0,05) у пацієнтів із виразкою. Ві6рометрія продемонструвала суттєве зниження чутливості в цілому по групі, причому якщо у хворих без виразки цей показник дорівнював 3,6+0,1 ум.од., то за умов наявності виразково-некротичного процесу він складав лише 0,9+0,03 ум.од. У всіх хворих на ЦД 1 типу з виразкою мала місце діабетична ретинопатія, яка у 70% випадків була проліферативною, а в 30% - непроліферативною. Для порівняння слід зауважити, що тільки у 41,6% хворих на ЦД 1 типу без виразки було виявлено ретинопатію. У 80% хворих спостерігалась дисліпідемія при цьому рівні бета-ліпопротеїдів, триглцеридів і холестерину були достовірно вищими у пацієнтів з наявністю виразково-некротичного процесу.
Хворі на ЦД 2 типу з ускладненою формою синдрому діабетичної стопи також були переважно чоловіки (співвідношення чоловіків та жінок складало 7:4), але, на відміну від хворих на ЦД 1 типу, не було виявлено різниці між групами з виразками та без них за такими показниками, як вік, тривалість захворювання, прояви дисліпідемії. В групі хворих з ЦД 2 типу найбільш вагому різницю між підгрупами з виразками та без таких було виявлено за такими показниками, як зниження вібраційної чутливості, наявність супутньої макроангіопатії та зниження рівня С- пептиду.
Для визначення ефективності різних доз препарату еспа-ліпон всі хворі, залежно від проявів синдрому діабетичної стопи, також були розподілені на дві. групи. До 1-ї групи увійшли пацієнти без виразково-некротичних дефектів стоп, до 2-ї- з наявністю таких. Кожну групу було розподіллено на підгрупи залежно від призначеної внутрішньовенно дози еспа-ліпону: А - 600 мг, Б – 900 мг, В – 1200 мг на добу. Курс лікування хворих підгрупи А складався з призначення еспа-ліпону по 600 мг/добу в/в № 10, а потім по 600 мг/ добу per os № 60. Пацієнти підгрупи Б отримували по 900 мг/добу в/в № 10, потім по 600 мг/добу per os № 60 а підгрупи В - по 1200 мг/добу в/в № 10, потім по 600 мг/добу per os № 60 еспа-ліпону. Всі хворі 2-ї групи отримували антибактеріальну терапію у зв'язку з виразково-некротичними ураженнями стоп.
Групи хворих, які отримували різні дози еспа- ліпону, були однаковими за віком, анамнезом та станом компенсації діабету, тривалістю та клінічними проявами діабетичної полінейропатії. Не відзначено також помітних відмін і серед інших клінічних характеристик та лабораторних параметрів у цих пацієнтів.
Результати та обговорення
Оцінку переносимості та клінічної ефективності терапії у всіх хворих проводили на 21-28-й день та через 3 місяці після початку лікування. Ефективність визначали за зменшенням больового синдрому, використовуючи аналогову 10-балову шкалу, покращенням вібраційної чутливості, а за умов наявності виразково-некротичного процесу - за зникненням супутнього целюліту та набряку тканин, очищенням рани від гнійного відділку, швидкістю загоєння рани, відновленням структури кісток. Динаміку зменшення больового синдрому та відновлення вібраційної чутливості через 21-28 діб від початку лікування та ефективність 3- місячного курсу терапії наведено на рис. 1-3.
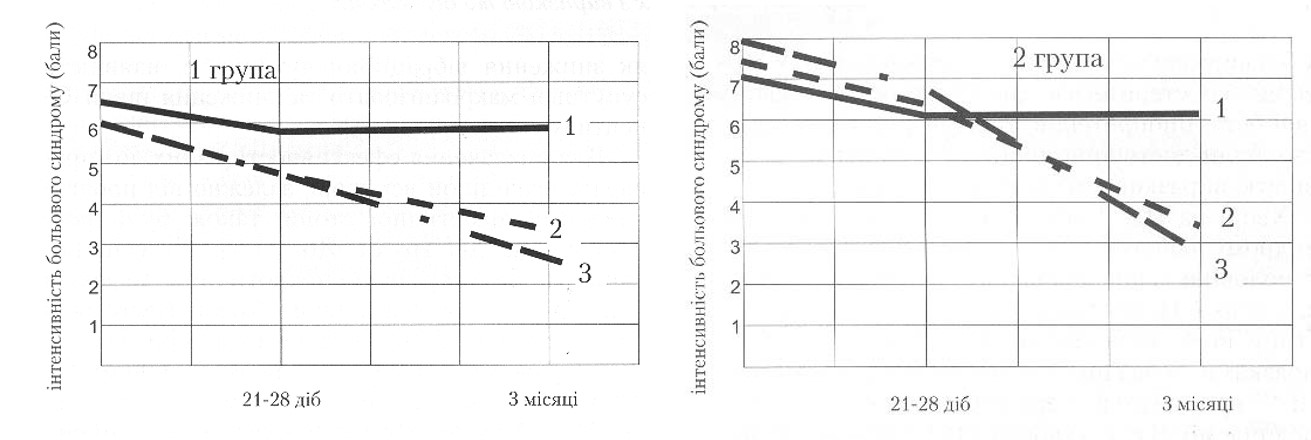
Рис.1. Динаміка больового синдрому у хворих на ЦД із синдромом діабетичної стопи без (1 група) та з (2 група) виразково-некротичними дефектами в ході лікування різними дозами еспа-ліпону: 1-600 мг/добу, 2 – 900 мг/добу, 3 – 1200 мг/добу
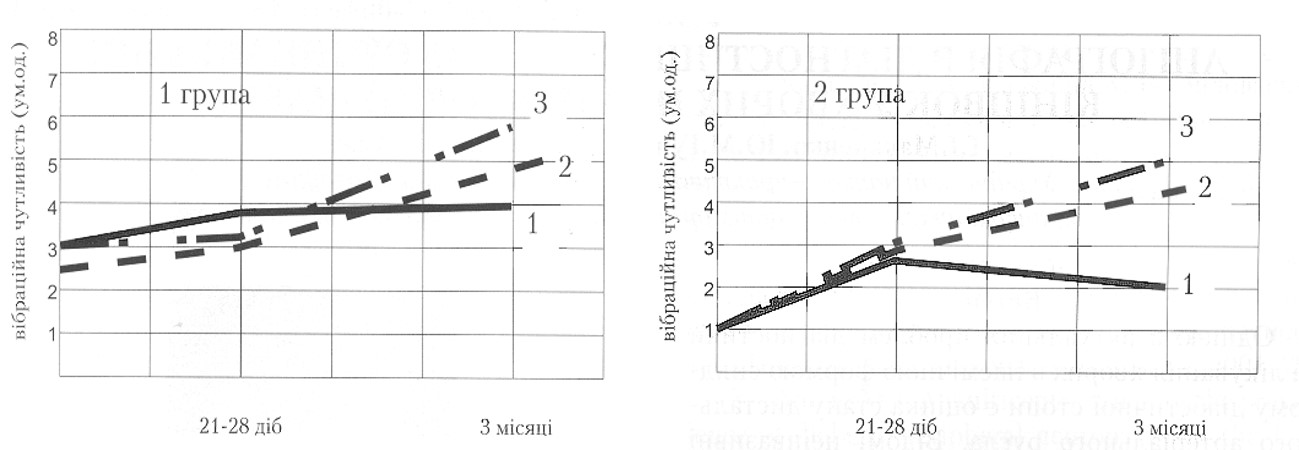
Рис. 2. Динаміка вібраційної чутливості у хворих на ЦД із синдромом діабетичної стопи без (1 група) та з (2 група) виразково-некротичними дефектами в ході лікування різними дозами еспа-ліпону: 1-600 мг/добу, 2 – 900 мг/добу, 3 – 1200 мг/добу.
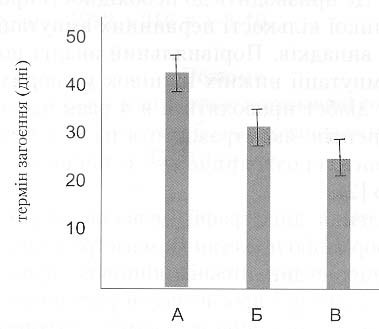
Рис. 3. Терміни загоєння виразок у хворих на ЦД Із синдромом діабетичної стопи при лікуванні Різними дозами еспа-ліпону : А – 600 мг/добу, Б – 900 мг/добу, В – 1200 мг/добу.
Таким чином, як видно з даних, наведених вище, внутрішньовенне введення еспа-лiпону в дозах 900 та 1200 мг/добу (групи 1-Б, В, 2-Б, В) призвело до помітного скорочення часу загоєння виразково-некротичних дефектів, зменшенню скарг на 6іль у нижніх кінцiвках у порівнянні з групами 1-А та 2-А. Визначена позитивна динаміка призвела до значного покращення самопочуття хворих та якості їх життя, дозволила зменшити загрозу ампутації. Частота побічних ефектів (збільшення артеріального тиску, нудота) від застосування різних доз еспа-ліпону була незначною та не призвела до відміни препарату в жодному з випадків.
Висновки
- Лікування полiнейропатії нижніх кінцівок у хворих на цукровий діабет потребує призначення еспа-ліпону за стандартною схемою: 600 мг внутрішньовенно крапельно № 10-20, потім 600 мг per os № 60.
- Внутрішньовенне крапельне введення еспа- ліпону в дозах 900 та 1200 мг/добу з наступним вживанням 600 мг/добу перорально у ком- плексному лікуванні дозволяє досягти помітно швидшого зменшення клінічних проявів діабетичної полінейропатії нижніх кінцівок та достовірного скорочення термінів загоєння виразково-некротичних дефектів, що надає можливості значного зменшення термінів перебування хворого в стаціонарі, зниження ступеня інвалідізації пацієнтів внаслідок синдрому діабетичної стопи.
- Проведене дослідження продемонструвало, що парентеральне введення еспа-ліпону як у дозі 600 мг, так і 900 та 1200 мг на добу однаково добре переноситься хворими та не викликає достовірно значущих побічних ефектів.
- Все викладене вище дозволяє рекомендувати застосування еспа-ліпону в дозах 900 та 1200 мг/добу внутрішньовенно крапельно з наступним вживанням 600 мг/добу перорально протягом 2 місяців за умов лікування хворих на цукровий діабет з діабетичною полінейропатією у випадках наявності синдрому діабетичної стопи, ускладненого виразково-некротичним процесом.
Література
- Vinik A.T., Mitchell B.D., Leichter S.B., Wagnes A.L., et al. Epidemiology of the Complications of Diabetes. In; Leslie R.D.6., Robbins D.S. (eds) Diabetes Clinical Science in Practice. Cambridge University Press, Cambridge. P.221-287.
- Armstrong D.G., Laverly L.A., Harkless L.B. Validation of a diabetic wound classification system. The contribution of depth, infection, and ischemia to risk of amputation.// Diabetes Care.- 1998.-V.21.-p.855-859.
- Eds Boulton A.J.M., Connor H., Cavanagh P.R. The Foot in Diabetes//1997.243 p.
- Levitt N.S., Stransberry R.B., Wychnyak S., Vinik A.I. Natural progression of autonomic neuropathy and autonomic function tests in a cohort of IDDM//Diabetes Care.-1996.-V.19/- p.751-754.
Підготували О.С.Ларін, О.В.Савран, В.Н.Скибун, Д.Г.Когут, О.Я.Гирявенко
Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, Київ
Опубліковано в журналі «Клінічна ендокринологія та ендокринна хірургія» №2(3)'2003


